Corona-Impfstoff BNT162b2 (COMIRNATY) von BioNTech/Pfizer
23. Januar 2021Der mRNA-Impfstoff BNT162b2 von BioNTech/Pfizer wurde für die Prävention von COVID-19 unter dem Namen COMIRNATY und der INN Bezeichnung Tozinameran in der EU zugelassen. Die Zulassung gilt für die aktive Immunisierung bei Personen ab dem 16. Lebensjahr zum Schutz vor COVID-19. Hier finden Sie alle wichtigen Informationen.
Aktuelles
- Neue Stabilitätsdaten zeigen, dass Comirnaty auch im verdünnten Zustand innerhalb der sechs Stunden Haltbarkeit transportfähig ist. Erschütterungen während des Transports sind allerdings unbedingt zu vermeiden.
- Die EMA bestätigt, dass aus einer Durchstechflasche sechs Dosen entnommen werden dürfen. Reste aus verschiedenen Ampullen dürfen allerdings nicht gepoolt werden.
- Die EU-Kommission hat einen Vertrag über weitere 300 Millionen Dosen des Impfstoffs abgeschlossen.
- In Marburg wird derzeit ein neuer Produktionsstandort von BioNTech aufgebaut. Durch diesen könnte die Impfstoffproduktion stark ausgebaut werden.
- Eine neue Studie zeigt, dass Comirnaty auch vor den Mutationen des Virus schützen kann.
- Die Ständige Impfkommission empfiehlt das in der Fachinformation vorgegebene Impfintervall einzuhalten.
Was ist BNT162b2 und wofür wird es angewendet?
BNT162b2 ist ein mRNA-Impfstoff von BioNTech/Pfizer zur aktiven Immunisierung von Personen ab 16 Jahren zur Verhinderung der Erkrankung COVID-19, welche durch das SARS-CoV-2-Virus verursacht wird. Der Impfstoff wird in der EU unter dem Namen COMIRNATY vermarktet. Der Name vereint die Wörter „COVID-19”, „mRNA”, „Community” (engl. für „Gemeinschaft”) und „Immunity” (engl. für „Immunität”).
Es handelt sich um eine Mehrfachdosis-Durchstechflasche, die vor der Anwendung verdünnt werden muss. Die Durchstechflasche (0,45 ml) enthält bis zu 6 Dosen 30 Mikrogramm BNT162b2-RNA (eingebettet in Lipidnanopartikel).
Die hochaufgereinigte einzelsträngige 5′-capped messenger-RNA (mRNA) wurde durch zellfreie in-vitro-Transkription von den entsprechenden DNA-Matrizen hergestellt und codiert für das virale Spike (S)-Protein von SARS-CoV-2.
Wie wird BNT162b2 angewendet?
BNT162b2 wird intramuskulär in den Deltamuskel in zwei Dosen mit jeweils 0,3 ml im Abstand von 21 Tagen verabreicht. Personen, die eine Dosis des Impfstoffs BNT162b2 erhalten haben, sollen auch eine zweite Dosis des mit BNT162b2 erhalten, um die Impfserie abzuschließen.
- CAVE: Injizieren Sie den Impfstoff nicht intravaskulär, subkutan oder intradermal!
- Um die Rückverfolgbarkeit von biologischen Arzneimitteln zu verbessern, sollten der Name und die Chargennummer des verabreichten Produkts klar aufgezeichnet werden.
- 7 Tage nach der zweiten Impfstoffdosis kann mit einem Impfschutz gerechnet werden.
- Applikation idealerweise in 0,5- oder 1-ml-Spritze
Nach der Impfung wird eine engmaschige Beobachtung von mindestens 15 Minuten empfohlen. Eine zweite Dosis des Impfstoffs sollte nicht an Personen verabreicht werden, bei denen eine Anaphylaxie nach der ersten Dosis von Comirnaty aufgetreten ist.
Wie wird BNT162b2 gelagert?
Ultra-Tieftemperatur-Gefrierschrank: Maximal 6 Monate
Thermoversandbehälter: Maximal 15 Tage
Kühlschrank (2-8°C): Maximal 120 Stunden
Genaue Handhabung und Applikation
Die gefrorenen Fläschchen sollten zum Auftauen auf 2°C bis 8°C gebracht werden. Alternativ können gefrorene Fläschchen auch aufgetaut und bei Temperaturen von bis zu 25°C für maximal zwei Stunden aufbewahrt werden. Wenn der unverdünnte Impfstoff aus dem Gefrierschrank genommen wird, hat er eine maximale Haltbarkeit von bis zu 5 Tagen (120 Stunden) bei 2°C bis 8°C und zusätzliche 2 Stunden bei Temperaturen von bis zu 25°C zur Vorbereitung der Verdünnung.
Wann darf der Impfstoff nicht mehr genutzt werden?
- Nach Temperaturschwankungen
- Bei negativem Ergebnis der Sichtkontrolle des aufgetauten Konzentrats oder des verdünnten Impfstoffes
- Wenn der verdünnte Impfstoff wieder eingefroren wurde
Schritt 1
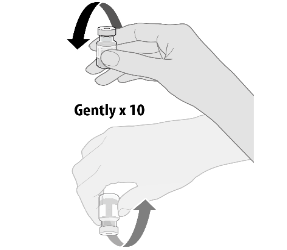
- Auftauen: Empfehlung: im Kühlschrank ca. 3 Stunden, alternativ 30 Minuten bei Raumtemperatur
- Wenn das aufgetaute Fläschchen Raumtemperatur erreicht hat, drehen Sie es vor der Verdünnung vorsichtig 10 Mal um. Nicht schütteln.
- Vor der Verdünnung sollte der Impfstoff als cremefarbene Lösung ohne sichtbare Partikel vorliegen.
- Entsorgen Sie den Impfstoff, wenn Partikel oder Verfärbungen vorhanden sind.
Schritt 2
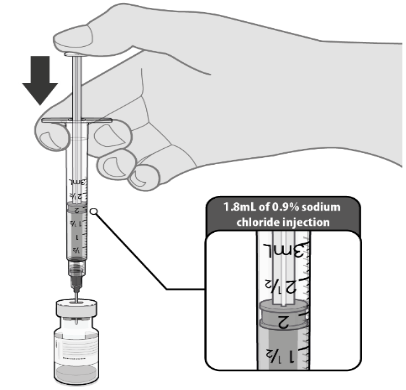
- Der aufgetaute Impfstoff muss in seiner ursprünglichen Durchstechflasche mit 1,8 ml Natriumchloridlösung 9 mg / ml (0,9%) zur Injektion unter Verwendung einer 21-Gauge-Nadel (Farbe nach EN ISO 6009 dunkelgrün) oder dünneren Nadel mit einer 2 ml Spritze aseptisch verdünnt werden.
- CAVE: Nicht konservierte Natriumchloridlösung 9 mg/ml (0,9%) für Injektionszwecke ist das einzige Verdünnungsmittel, das verwendet werden sollte. Dieses Verdünnungsmittel ist nicht im Impfkarton enthalten.
Schritt 3
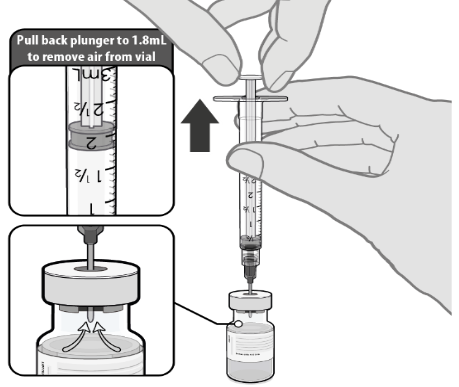
- Bevor die Nadel aus dem Fläschchen entfernt wird, muss der Fläschchendruck ausgeglichen werden, indem 1,8 ml Luft in die leere Verdünnungsmittelspritze gezogen werden.
Schritt 4

- Drehen Sie die verdünnte Lösung vorsichtig 10 Mal um. Nicht schütteln. Der verdünnte Impfstoff sollte als cremefarbene Lösung ohne sichtbare Partikel vorliegen.
- Entsorgen Sie den verdünnten Impfstoff, wenn Partikel oder Verfärbungen vorhanden sind.
- Die verdünnten Fläschchen sollten mit dem Verdünnungsdatum sowie der Verdünnungszeit gekennzeichnet und zwischen 2°C und 25°C gelagert werden.
- Die Applikation soll so bald wie möglich und innerhalb von 6 Stunden nach der Verdünnung erfolgen.
- Haltbarkeit des vorbereiteten Impfstoffes: 6 Stunden bei bis zu 30°C
Schritt 5
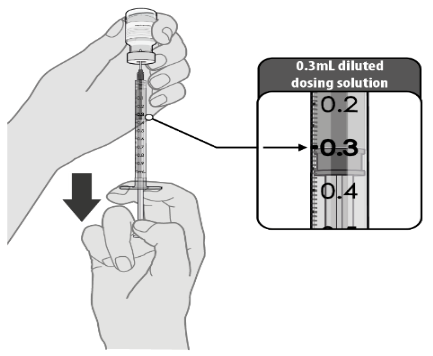
- Nach der Verdünnung enthält das Fläschchen 5 Dosen a 0,3 ml. Ziehen Sie die erforderliche 0,3 ml-Dosis des verdünnten Impfstoffs mit einer sterilen Nadel und einer 1-ml-Luer-Spritze heraus und verabreichen Sie sie.
- Auf Verfärbungen oder Partikel prüfen
- Nicht verwendeter Impfstoff sollte 6 Stunden nach der Verdünnung verworfen werden.
- Bislang galt, dass BNT162b2 nach der Verdünnung nicht mehr transportiert werden solle. BioNTech hat jedoch neue Stabilitätsdaten vorgelegt, die zeigen, dass die mRNA auch im verdünnten Zustand innerhalb der sechs Stunden Haltbarkeit transportfähig ist. Erschütterungen während des Transports sind allerdings unbedingt zu vermeiden.
Dosierung
Die Dosis von BNT162b2 beträgt je 0,3 ml der Verdünnung (30 µg BNT162b2 RNA) im Abstand von 21 Tagen.
Wie wirkt BNT162b2?
Der Nukleosid-modifizierte Messenger-RNA-Impfstoff BNT162b2 wird in Lipidnanopartikeln formuliert, die die Abgabe der RNA in Wirtszellen ermöglichen, damit die Expression des SARS-CoV-2 S-Antigens erfolgen kann. Der Impfstoff löst sowohl neutralisierende Antikörper als auch zelluläre Immunantworten gegen das Spike (S)-Antigen aus, was zum Schutz vor COVID-19- beitragen kann.
Gegenanzeigen
Der Impfstoff darf nicht angewendet werden bei akuter Erkrankung mit Fieber oder bei Personen unter antikoagulativer Therapie, bei denen eine intramuskuläre Applikation kontraindiziert ist (es sei denn, der potenzielle Nutzen überwiegt eindeutig das Risiko der Verabreichung).
Weiterhin ist die Impfung kontraindiziert bei Überempfindlichkeit gegen den Wirkstoff oder einen der Hilfsstoffe:
- ALC-0315 = (4-Hydroxybutyl) azandiyl) bis (hexan-6,1-diyl) bis (2-hexyldecanoat)
- ALC-0159 = 2-[(Polyethylenglykol)-2000]-N,N-Ditetradecylacetamid
- 1,2-Distearoyl-sn-glycero-3-phosphocholin
- Cholesterol
- Kaliumchlorid
- Kaliumdihydrogenphosphat
- Natriumchlorid
- Dinatriumhydrogenphosphatdihydrat
- Saccharose
Schwangerschaft
Es liegen keine oder nur begrenzte Daten zur Anwendung von BNT162b2 in der Schwangerschaft vor. Tierexperimentelle Studien lassen nicht auf direkte oder indirekte schädliche Wirkungen in Bezug auf Schwangerschaft, embryonale/fötale Entwicklung, Geburt oder postnatale Entwicklung schließen.
Stillen
Es ist nicht bekannt, ob BNT162b2 in die Muttermilch übergeht.
Fertilität
Tierexperimentelle Studien lassen nicht auf direkte oder indirekte schädliche Wirkungen in Bezug auf die Reproduktionstoxizität schließen.
Kinder
Die Sicherheit und Wirksamkeit von BNT162b2 wurde bei Kindern unter 16 Jahren noch nicht nachgewiesen.
Nebenwirkungen
Die häufigsten Nebenwirkungen bei Probanden der klinischen Studien ab 16 Jahren waren:
- Schmerzen an der Injektionsstelle (>80%)
- Müdigkeit (>60%)
- Kopfschmerzen (>50%)
- Myalgie (>30%)
- Schüttelfrost (>30%)
- Arthralgie (>20%)
- Pyrexie (>10%)
Diese waren gewöhnlich leicht oder mäßig intensiv und klangen innerhalb weniger Tage nach der Impfung ab. Zur symptomatischen Behandlung können analgetische und/oder antipyretische Arzneimittel wie Paracetamol verwendet werden.
Wechselwirkungen
- Es wurden keine Interaktionsstudien mit BNT162b2 durchgeführt. Die gleichzeitige Verabreichung von BNT162b2 mit anderen Impfstoffen wurde nicht untersucht.
- Mischen Sie BNT162b2 nicht mit anderen Impfstoffen/Produkten in derselben Spritze.
- Immunschwache Personen, einschließlich Personen, die eine immunsuppressive Therapie erhalten, können eine verminderte Immunantwort auf den Impfstoff haben. Es liegen allerdings keine Daten zur gleichzeitigen Anwendung mit Immunsuppressiva vor.
Studienlage
Präklinik
In präklinischen Studien lösten BNT162b1 und BNT162b2 vorteilhafte Virusantigen-spezifische CD4+ und CD8+ T-Zell-Antworten und in verschiedenen Tiermodellen hohe Mengen an neutralisierenden Antikörpern aus. Außerdem zeigten die Kandidaten einen vorteilhaften, schützenden Effekt in Primaten in einem SARS-CoV-2-Challenge-Modell. In einer präklinischen Studie an nicht-humanen Primaten verhinderte die Immunisierung der Tiere mit BNT162b2 eine Infektion mit SARS-CoV-2. Weiterhin zeigte die Vakzine schützende antivirale Effekte in Rhesusaffen sowie hohe Titer neutralisierender Antikörper und eine TH1-Zell-Antwort in Rhesusaffen und Mäusen.
In einem viralen Infektionsmodell erhielten Makaken zwei Injektionen mit je 100 µg BNT162b2 bzw. Salzlösung als Kontrolle. 55 Tage nach der zweiten Immunisierung wurden die Tiere intranasal (über die Nase) sowie intratracheal (über die Lunge) mit dem SARS-CoV-2-Virus in einer hohen Konzentration von ca. 1 Million sog. “plaque forming units” infiziert. Eine vorangegangene Immunisierung mit BNT162b2 reduzierte die Virusinfektion und es konnte keine virale RNA in den unteren Atemwegen der immunisierten Tiere nachgewiesen werden. In den meisten nicht-immunisierten Tieren (Salzlösung) wurde hingegen virale RNA detektiert.
Insbesondere induzierte BNT162b2 potente neutralisierende Antikörper in geimpften Makaken sowie Virusantigen-spezifische CD4+ und CD8+ T-Zell-Antworten. Rhesusaffen wurden an Tag 0 und Tag 21 (zwei Dosen) intramuskulär (IM) mit 30 µg oder 100 µg BNT162b2 bzw. Kontroll-Salzlösung geimpft. Nach der zweiten Immunisierung konnten im Serum der Rhesusaffen neutralisierende Antikörper mit einem geometrischen Titer-Mittelwert (geometric mean titer, GMT) von 962 (Tag 35 bei der 30 µg-Kohorte) oder 1.689 (Tag 28 bei der 100 µg-Kohorte) nachgewiesen werden.
Die neutralisierenden Antikörpertiter persistierten bis mindestens Tag 56, wobei die GMTs höher waren als die in einem Panel humaner Rekonvaleszenz-Seren.
Die Impfung mit BNT162b2 induzierte eine hohe Frequenz an CD4+ T-Zellen, die IFN-ɣ, IL-2 und TNF-α produzierten, hingegen waren fast keine IL-4-produziertenden CD4+ T-Zellen detektierbar. Dies deutet auf eine stark TH1-basierte Zellantwort hin, einem Immunprofil, von dem angenommen wird, dass es einen sicheren Impfstoff unterstützt. BNT162b2 induzierte zudem auch Spikeprotein-spezifische, IFN-ɣ-produzierende CD8+ T-Zell-Antworten, von denen angenommen wird, dass sie einen antiviralen Effekt unterstützen.
In einem präklinischen Mausmodell generierte eine einzelne IM-Immunisierung mit BNT162b2 (0,2 µg, 1 µg oder 5 µg) B- und T-Zell-Antworten in BALB/c-Mäusen sowie neutralisierende SARS-CoV-2-Pseudovirus-Antikörper, deren Titer bis Tag 28 stetig anstiegen (dem letzten Tag der Titer-Messung). CD4+ und CD8+ T-Zellen aus Splenozyten, welche aus mit BNT162b2 geimpften Mäusen isoliert wurden, waren stark positiv für IFN-ɣ und IL-2 und produzierten hohe Level an TH1-Zytokinen aber nur kleine Mengen TH2-Zytokine. Dies weist auf eine robuste, verstärkt TH1-gerichtete, adaptive T-Zell-Immunantwort hin.
NCT04380701
Die Studie NCT04380701 war die erste klinische Prüfung eines COVID-19-Impfstoffkandidaten in Deutschland.
- 456 Teilnehmer
- Start 23. April 2020
- Phase I/II
Die Studie besteht aus zwei Teilen: Teil A befasst sich mit der Dosisfindung und Teil B besteht aus der Rekrutierung von Expansionskohorten mit Dosierungen, die aus Teil A generiert wurden.
Die Impfstoffe BNT162a1, BNT162b1, BNT162b2 und BNT162c2 wurden unter Verwendung eines Prime / Boost-Regimes verabreicht. Der Impfstoff BNT162c2 wurde als Einzeldosis verabreicht.
Ziele:
Um die optimale Dosis für die weiteren Studien zu finden umfasste die Kohorte zur Dosisfindung der Phase-I/II-Studie einen Dosisbereich von 1 µg bis 100 µg. Außerdem sollten die Sicherheit und Immunogenität des Impfstoffes untersucht werden. Ziel der Studie ist es, die Auswirkungen einer wiederholten Impfung für die drei Impfstoffkandidaten, welche uridinhaltige mRNA (uRNA) oder nukleosidmodifizierte mRNA (modRNA) beinhalten, zu untersuchen. Der vierte Impfstoffkandidat, der selbstamplifizierende mRNA (saRNA) enthält, wird nach der Verabreichung einer einzigen Impfstoffdosis bewertet. Probanden mit einem höheren Risiko für einen schweren Verlauf einer COVID-19-Infektion werden in den zweiten Teil der Studie aufgenommen.
Ergebnisse:
Vorläufige klinische Ergebnisse von rund 120 Probanden zeigten ein vorteilhaftes Gesamtverträglichkeitsprofil von BNT162b2 verglichen mit BNT162b1. Systemische Nebenwirkungen wie Fieber, Müdigkeit und Schüttelfrost waren bei BNT162b2 nur leicht bis moderat ausgeprägt und traten nur vorübergehend auf (1-2 Tage). Es gab keine schwerwiegenden Nebenwirkungen.
Zwei 30 µg-Dosen von BNT162b2 führten zu vergleichbaren neutralisierenden Antikörper-Mittelwerten (geometric mean titers, GMTs) wie die des Impfstoffkandidaten BNT162b1. Ibei älteren Probanden mit einem Alter von 65-85 Jahren lösten zwei Dosen über je 30 µg, die im Abstand von drei Wochen appliziert wurden, höhere neutralisierende Antikörper-GMTs aus, als in einem Panel aus 38 Rekonvaleszenz-Seren von Patienten, die sich von einer COVID-19-Erkrankung erholt hatten.
Mit BNT162b2 geimpfte Probanden wiesen verglichen mit BNT162b1 eine vorteilhafte Breite von Epitopen auf, die in SARS-CoV-2-Antigen-spezifischen T-Zell-Antworten erkannt werden. BNT162b2 zeigte eine gleichzeitige Induktion von hohen Leveln an CD4+ and CD8+ T-Zell-Antworten auf.
Weiterhin löste BNT162b2 T-Zell-Antworten gegen die Rezeptor-Bindungs-Domäne (RBD) und gegen den restlichen Teil des Spike-Glykoproteins aus, der nicht im BNT162b1-Impfstoffkadidaten enthalten ist. Die Unternehmen nehmen an, dass die Erkennung weiterer Spike-Epitope durch T-Zellen des Immunsystems das Potenzial haben kann, konsistentere Immunantworten in vielfältigen Bevölkerungsgruppen sowie in älteren Erwachsenen zu erzielen.
NCT04368728
Die Studie NCT04368728 ist eine randomisierte, verblindete, Placebo-kontrollierte Phase-II/III-Studie, die die Daten zu Sicherheit, Immunantwort und Wirksamkeit für den Zulassungsantrag evaluiert.
- 43998 Teilnehmer
- Start: 29.April 2020
- Phase II/III
Ziele:
Die primären Endpunkte der Studie beinhalten die Prävention einer COVID-19-Infektion in Teilnehmern, die vor der Impfung noch keine SARS-CoV-2-Infektion hatten, sowie die Prävention in Teilnehmern unabhängig von einer vorangegangen SARS-CoV-2-Infektion.
Zu den sekundären Endpunkten gehört die Prävention schwerer COVID-19-Infektionen in diesen Teilnehmergruppen. Die Studie wird weiterhin die Prävention einer Infektion mit SARS-CoV-2 untersuchen, dem Virus, das COVID-19 verursacht. Die primäre Wirksamkeitsanalyse wird eine ereignisgesteuerte Untersuchung basierend auf der Anzahl an Probanden mit symptomatischer COVID-19-Infektion sein. Das Studiendesign ermöglicht vorläufige Zwischenanalysen sowie unverblindete Bewertungen durch ein unabhängiges, externes Data Monitoring Committee.
Ergebnisse:
Die Auswertung der Daten zeigte in Probanden ohne vorherige SARS-CoV-2-Infektion einen 95%igen Impfschutz (p<0.0001). Auch in Probanden mit oder ohne vorheriger SARS-CoV-2-Infektion konnte ein Impfschutz erreicht werden. In beiden Fällen wurde der Impfschutz sieben Tage nach der zweiten Dosis ermittelt. Die Abschlussanalyse wurde, basierend auf dem Studienprotokoll, nach 170 bestätigten COVID-19-Fällen durchgeführt.
Davon wurden 162 Fälle in der Placebogruppe und 8 Fälle in der BNT162b2-Impfstoff-Gruppe nachgewiesen. Die Wirksamkeit der Impfung war über alle Alters- und Geschlechtsgruppen in der gesamten diversen Studienpopulation konsistent. Der Impfschutz bei Erwachsenen über 65 Jahren lag bei über 94%.
In der Studie traten insgesamt 10 schwere COVID-19-Verläufe auf. Davon wurden 9 in der Placebogruppe und einer in der BNT162b2-Gruppe beobachtet. Bislang konnte das Data Monitoring Committee keine schwerwiegenden Nebenwirkungen feststellen und auch eine Untersuchung der entblindeten Daten zur Impfstoffreaktion in einer randomisierten Subgruppe der finalen Phase-II/III-Analyse mit mindestens 8.000 der über 18-jährigen Probanden zeigte, dass der Impfstoff gut verträglich ist.
Die meisten Nebenwirkungen traten nur vorübergehend auf. Die einzigen schweren Nebenwirkungen (3. Grades), die in mehr als 2% der Probanden nach der ersten oder zweiten Impfung auftraten, waren Erschöpfung mit 3,8% sowie Kopfschmerzen mit 2,0% nach der zweiten Dosis. Wie auch schon in früheren Analysen traten bei älteren Studienteilnehmern weniger und schwächer ausgeprägte Nebenwirkungen auf.
Haltbarkeiten im Überblick
Zustand |
Voraussetzung |
Zeit/Haltbarkeit |
Transport |
| Gefroren | Lagerung im Ultra-Tieftemperatur-Gefrierschrank bei -75°C (±15°C) (Empfehlung) | Maximal 6 Monate | Unbegrenzt |
| Lagerung im Thermoversandbehälter bei -75°C (±15°C) | Maximal 15 Tage (bei Auffülung mit Trockeneis) | Unbegrenzt bei ausreichend Trockeneis | |
| Auftauprozess | Lagerung im Kühlschrank/Kühlbox bei 2°C bis 8°C (Empfehlung) | Dauer ca. 3 Stunden | Maximal erlaubte Transportzeit 12 Stunden bei 2°C bis 8°C (Transport kann unterbrochen und später fortgesetzt werden) |
| Lagerung bei Raumtemperatur bei 2°C bis 30°C | Dauer ca. 30 Minuten (einzelne Durchstechflaschen) | Kein Transport | |
| Aufgetaut | Lagerung im Kühlschrank/Kühlbox bei 2°C bis 8°C (Empfehlung) | Maximal 5 Tage (120 Stunden) | Maximal erlaubte Transportzeit 12 Stunden bei 2°C bis 8°C (Transport kann unterbrochen und später fortgesetzt werden) |
| Lagerung bei Raumtemperatur bei 2°C bis 30°C | Maximal 2 Stunden | Maximal erlaubte Transportzeit 30 Minuten bei Raumtemperatur (bis zu 30°C) | |
| Verdünnt | Anwendung nach Verdünnung bei Raumtemperatur bei 2°C bis 30°C | Maximal 6 Stunden | Nicht empfohlen |